来凯医药一项新的Ib/III期全球多中心临床研究在
- 比原计划提前一个月在中国和美国同时启动临床试验
- HR+/HER2- 乳腺癌患者占比最大,肿瘤耐药后的治疗选择是亟待解决的难点之一。
- Afuresertib临床新药试验已覆盖4癌症类型
中国上海和美国新泽西8月25日, 2021/美通社/ - 莱凯医药宣布,继美国食品药品监督管理局(FDA)6月19日获批后,中国国家药品监督管理局(CDE)也于8月17日批准了莱凯医药新的临床试验:一项新的临床试验。处于临床开发阶段的候选药物 afresertib (LAE002) 联合抗雌激素药物氟维司群,用于局部晚期或转移性激素受体阳性/人表皮生长因子 2 受体阴性乳腺癌 w在此标准治疗失败的患者(以下简称 HR+/HER2-)Ib/III 期临床试验研究。
到目前为止,这项全球多中心临床研究比原计划提前一个月在中国和美国同步启动。这一快速获批也意味着,在 afuresertib 联合氟维司群联合治疗在 Ib 期研究中获得可靠的安全性数据后,可以尽快启动 3 期全球注册研究。
Afuresertib新药临床试验覆盖率4癌症类型
< p > Afuresertib (LAE002) 是莱臣从诺华引进全球独家权利并已证明临床结果的新候选药物(Proof of Concept)。是新一代小分子泛AKT激酶强效抑制剂。目前,Afuresertib已在全球4种癌症类型获得临床研究:涵盖卵巢癌、前列腺癌、三阴性乳腺癌、HR+/HER2-乳腺癌。
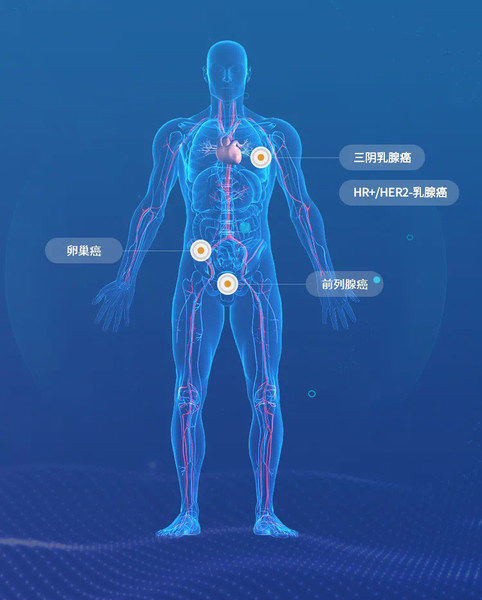
莱凯医药处于临床开发阶段1新药候选药物Afuresertib现已收获全球4种癌症临床研究
在联合治疗方面,现有4项临床试验与化疗药物“携手”,靶向药物和肿瘤免疫药物PD-L1单克隆抗体,下一步将是afuresertib和PD-1单克隆抗体联合临床研究。
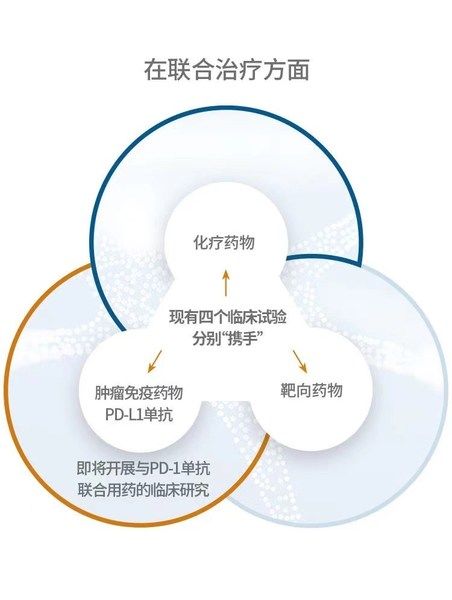
Afresertib 联合治疗概览 span>
努力解决HR+/HER2-抗乳腺癌的需要
< p> 乳腺癌是全球女性中最常见的癌症。中国约62%的乳腺癌患者属于HR+/HER2-[1],而美国患者中此类分子亚型的比例高达68%[2 ]。虽然大多数这些乳腺癌患者最初可以从一线/二线抗激素治疗和CDK4/6抑制剂或化疗中获益,但经过一段时间后,大多数癌症患者可能会对治疗产生耐药性。肿瘤耐药后的治疗选择一直是各种乳腺癌临床研究致力于解决的难点之一。
"HR+/HER2-占乳腺癌患者的最大比例。CDK4/6抑制剂耐药后的抗激素治疗和治疗是众多亟待解决的未满足医疗需求之一。1.这也是显着提高乳腺癌患者治疗效果、提高生活质量的最关键环节。”莱凯医药首席医疗官岳勇博士表示:“女性是一个家庭的核心和希望,目前已经有afuresertib多重联合治疗。在多种癌症耐药患者的临床试验中,抗-肿瘤的疗效和良好的安全性已经初步显现,尤其是针对女性特有的卵巢癌和乳腺癌。我们希望这些联合治疗能够给患者带来新的希望,让医生在面对这些难治性耐药的肿瘤时有更多更好的选择。患者。”
永正AKT酶抑制剂全球赛道“金牌”
“临床批件比原计划提前一个月获批,充分体现了国家药监局对乳腺癌的高效抗药??性,是对未来新一代治疗新药的期待和关注。时间,也凸显了强大的执行力莱凯医药中美团队的合作,有望让乳腺癌患者更早受益于新药。”莱凯医药董事长兼首席执行官卢向阳博士表示:“在AKT酶抑制剂的全球轨道上,莱凯医药目前处于第一梯队。我们正在加快多项临床试验,希望afresertib有实力赢得世界一流的金牌。。”
[1] Li, ZS, et al., 乳腺癌亚型和中国女性可手术原发性乳腺癌的生存率。中国癌症研究杂志,2011. 23(2): p. 134-9.
[2] SEER癌症统计数据:女性乳腺癌亚型。国家癌症研究所。 医学博士贝塞斯达。可从:
相关链接:
文章来源:《世界临床药物》 网址: http://www.sjlcywzz.cn/zonghexinwen/2021/0825/1527.html