1月份临床试验数据分析显示——全球新开试验数
原标题:1月份临床试验数据分析显示——全球新开试验数环比再次下滑 肿瘤领域竞争依然激烈
□陈宇哲
根据美国Clinicaltrial数据库,2022年1月,全球新开展的由企业资本主导的临床试验总数为845项,再次出现下滑趋势,相较于前一月下降2.1%,但单月新增临床试验数量显著高于2021年月平均水平。
1月份,申报临床试验数量最多的企业(机构)为默沙东,共申报22项;其次为诺华,共申报19项;第三为阿斯利康,共申报18项。在开展临床试验的Top10热门企业中,申报数量增幅最大的是罗氏和Incyte Corporation,月增幅分别为160%和100%;新增临床试验数量较上月减少的企业有阿斯利康和辉瑞,其中辉瑞下降幅度大于阿斯利康,为37.5%。对比热门Top3临床试验申报大企业(即默沙东、诺华、阿斯利康)在临床适应症和药物类型方面的布局可知,3家大企业在临床适应症方面竞争更为激烈,其中竞争最激烈的是组织分类肿瘤治疗领域,其次为免疫系统疾病治疗领域。
具体来看,默沙东主要专注于可瑞达(Pembrolizumab)和MK-2140临床适应症的拓展。可瑞达是一种人源化抗体,用于癌症免疫治疗,靶点为PD-1。2017年,美国FDA批准该药用于治疗任何无法切除或伴有某些遗传异常(错配修复缺陷或微卫星不稳定性)的转移性实体瘤;MK-2140是一种新型抗体-药物偶联物。
诺华在组织分类肿瘤中的布局则主要是开展Tisagenlecleucel、PHE885和VAY736 3个研究项目。Tisagenlecleucel是一种治疗B细胞急性淋巴细胞白血病的药物,它使用人体自身的T细胞来对抗癌症(过继细胞转移);PHE885是一项评估用新型B细胞成熟抗原(BCMA)特异性嵌合抗原受体(CAR)基因工程的自体T细胞的可行性、安全性和初步抗肿瘤功效的研究;VAY736是BAFF受体抑制与B细胞耗竭相结合的双作用生物模式。
阿斯利康在组织分类肿瘤中的布局基于Osimertinib、Durvalumab和Datopotamab Deruxtecan这3个项目。Osimer tinib是一种用于治疗具有特定突变的非小细胞肺癌的药物,是第三代表皮生长因子受体酪氨酸激酶抑制剂,于2016年在欧盟获批;Durvalumab是一种抗肿瘤药物,属于抗PD-L1单克隆抗体;Datopotamab Deruxtecan能够有效靶向于滋养细胞表面抗原2(TROP2)受体,并内化到肿瘤细胞中,然后在细胞内运输到溶酶体并释放DXd,诱导体外表达TROP2的肿瘤细胞DNA损伤和凋亡。
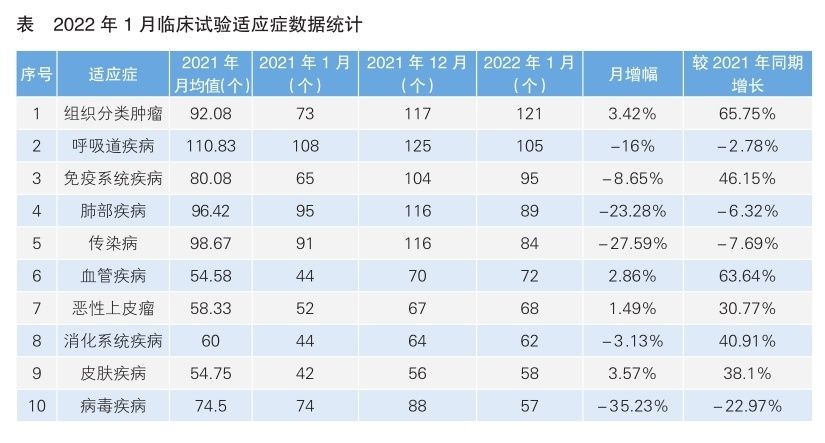
从1月份新增临床试验的热门适应症情况来看,组织分类肿瘤仍为最热门研发领域,试验数量为121项,相较于2021年12月份上升3.42%。1月份主要热门适应症的临床试验相较于2021年12月份大多呈现上升趋势,下降明显的热门适应症为病毒类疾病。推测新冠肺炎疫情对于临床试验的影响正在显著下降,临床试验正在逐步恢复常态。
从药物类型角度对新开展临床试验进行统计后发现,1月份新开展临床试验数量下降程度最明显的药物类型为疫苗,下降幅度为34.04%;可瑞达单品、抗炎药物、痛风药物的临床试验数量呈现上升趋势,其中可瑞达单品的月增幅最为明显,为40%。对比2021年同期水平,所有热门药物类型临床试验新增数量均呈现上升趋势。
对临床试验的申请国家和地区进行统计后发现,当月美国仍为临床试验开展最为主要的国家,其次是中国和德国。相较于2021年12月,临床试验申报的热门地区新开展试验数量普遍下降,仅有意大利和荷兰有上升趋势,月下降幅度最大的地区为中国和法国。对比2021年同期数据,所有热门国家和地区新增临床试验数量均出现下降。
(数据来源于美国Clinicaltrial数据库,标签间存在统计重复)(陈宇哲)
文章来源:《世界临床药物》 网址: http://www.sjlcywzz.cn/zonghexinwen/2022/0222/1942.html